Xử lý nước thải đối với các hợp chất Phốt pho tương đối phức tạp, không giống như nitơ, không có phốt pho ở dạng khí. Do đó, phốt pho phải được chuyển đổi sang dạng rắn và loại bỏ qua lắng, lọc, hoặc một số quá trình loại bỏ các chất rắn khác hoặc tách trực tiếp qua màng thích hợp.
Hợp chất Phospho trong môi trường nước thải tồn tại trong các dạng: Phospho hữu cơ, phosphate đơn (H2PO4–, HPO42-, PO43-) tan trong nước, polyphosphate hay còn gọi là phosphate trùng ngưng, muối phosphate và Phospho trong tế bào sinh khối.
Bảng bên dưới ghi các hợp chất Phospho chính và khả năng chuyển hóa của chúng.
Bảng. Hợp chất Phospho và khả năng chuyển hóa.
|
Hợp chất |
Khả năng chuyển hóa |
| Phospho hữu cơ | Phân hủy thành phosphate đơn và trùng ngưng |
| Phosphate đơn | Tan, phản ứng tạo muối, tham gia phản ứng sinh hóa. |
| Polyphotphat | Ít tan, có khả năng tạo muối tham gia phản ứng sinh hoá. |
| Muối photphat | Phần lớn không có độ tan thấp hình thành từ photphat đơn. |
| Phospho trong tế bào | Thành phần của tế bào hoặc lượng dư trong tế bào của một số vi khuẩn. |
Xử lý Phospho trong nước thải dựa trên các nguyên tắc sau:
– Kết tủa phosphate (đơn và một phần loại trùng ngưng) với các ion nhôm, sắt, canxi tạo ra các muối tương ứng có độ tan thấp và tách chúng ra dưới dạng chất rắn.
– Phương pháp sinh học dựa trên hiện tượng là một số loại vi sinh vật tích lũy lượng Phospho nhiều hơn mức cơ thể chúng cần trong điều kiện hiếu khí. Thông thường hàm lượng Phospho trong tế bào chiếm 1,5 – 2,5% khối lượng tế bào khô, một số loại có thể hấp thu cao hơn, từ 6 – 8%. Trong điều kiện yếm khí chúng lại thải ra phần tích lũy dư thừa. Quá trình loại bỏ Phospho dựa trên hiện tượng trên gọi là loại bỏ Phospho tăng cường. Phospho được tách ra khỏi nước trực tiếp thông qua thải bùn dư (vi sinh chứa nhiều Phospho) hoặc tách ra dưới dạng muối không tan sau khi xử lý yếm khí với một hệ kết tủa kèm theo (ghép hệ thống phụ).
– Tách các hợp chất Phospho đồng thời với các tạp chất khác qua quá trình màng thích hợp: màng nano, màng thẩm thấu ngược hoặc điện thẩm tích. Về nguyên tắc hiệu quả tách lọc qua màng có hiệu suất cao nhưng do giá thành quá đắt nên hầu như chưa thấy có ứng dụng trong thực tế.
I. Xử lý Phospho trong nước thải bằng phương pháp sinh học
Xử lý Phospho trong nước thải bằng phương pháp sinh học chủ yếu gồm 3 công nghệ sau:
– Xử lý Phospho bằng công nghệ A/O
– Xử lý Phospho bằng công nghệ PhoStrip
– Xử lý Phospho bằng công nghệ SBR
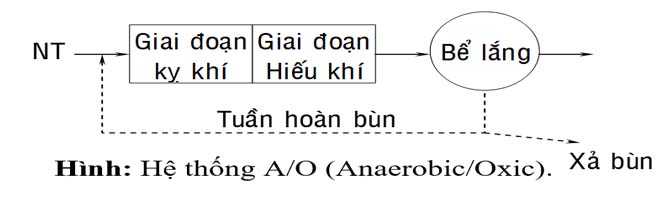
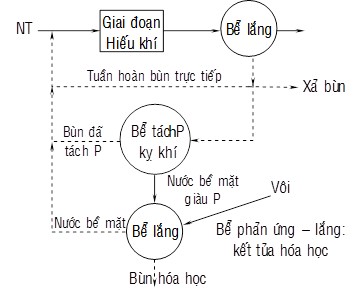
Hình: Hệ thống PhoStrip.Hình: Hệ thống A/O (Anaerobic/Oxic).
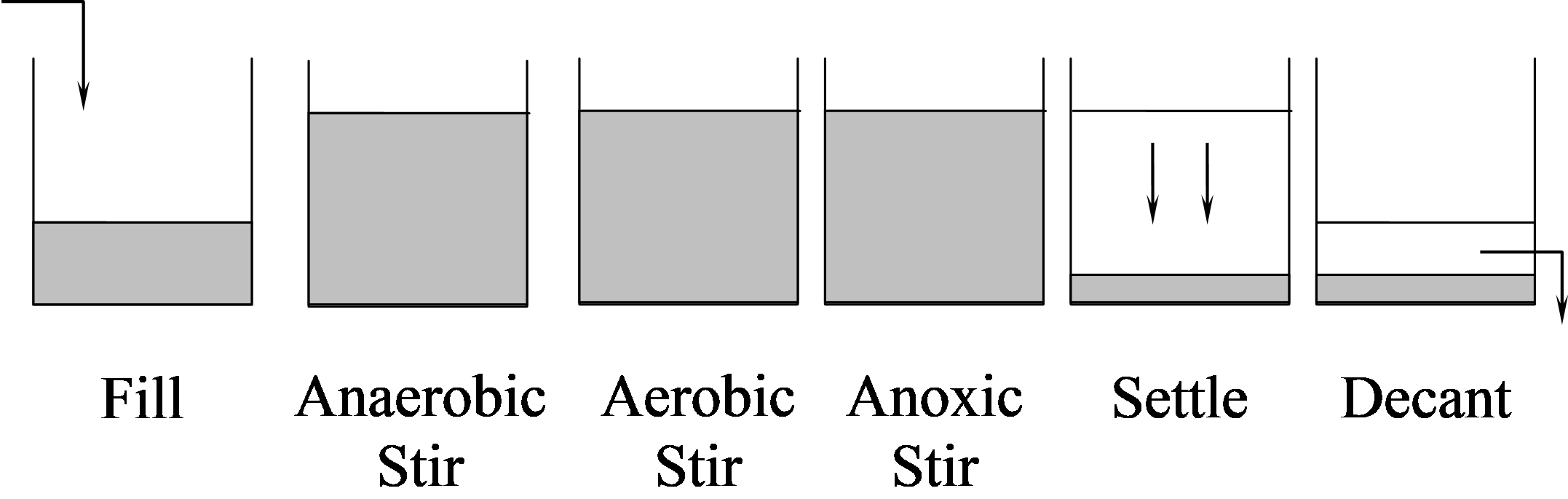
Hình: Hệ thống SBR.
SBR khử carbon, nitơ và phospho:
- Giải phóng P và tiêu thụ BOD : giai đoạn kỵ khí
- Tiêu thụ P : giai đoạn hiếu khí
- Chu kỳ : 3-24 giờ :
Bảng: Thông số thiết kế hệ thống xử lý Phospho bằng phương pháp sinh học
| Thông số | Đơn vị | Quá trình | ||
| A/O | PhoStrip | SBR | ||
| F/M | Ngày -1 | 0,2-0,7 | 0,1-0,5 | 0,15-0,5 |
| SRT (qc) | Ngày -1 | 2-25 | 10-30 | |
| MLSS | mg/L | 2.000-4.000 | 600-5.000 | 2.000-3.000 |
| HRT (q): | Giờ | |||
| – Kỵ khí | 0,5-1,5 | 8-12 | 1,8-3,0 | |
| – Hiếu khí | 1-3 | 4-10 | 1,0-4,0 | |
| Tuần hoàn bùn hoạt tính | % Lưu lượng xử lý | 25-40 | 20-50 | |
| Tuần hoàn nước | % Lưu lượng xử lý | 10-20 | ||
Bảng: Xử lý Phospho bằng phương pháp sinh học – Thuận lợi và không thuận lợi
| Quá trình | Thuận lợi | Không thuận lợi |
| A/O | – Sự vận hành đơn giản so với cá quá trình khác
– Bùn thải có thành phần Phospho cao (3-5%) và có giá trị làm phân bón – Thời gian lưu nước ngắn – Mức độ làm giảm hiệu quả của việc khử phopho có thể chấp nhận được, quá trình có lẽ đạt đến nitrat hóa hoàn toàn |
– Không có khả năng đạt đến mức độ cao của việc khử Phospho và nitơ đồng thời
– Trong điều kiện thời tiết lạnh quá trình vận hành không đảm bảo – Đòi hỏi tý số BOD/P cao – Thời gian lưu tế bào hiếu khí giảm thì đòi hỏi phải có thiết bị cung cấp oxy với tốc độ rất cao – Sự linh động kiểm soát quá trình bị giới hạn |
| PhoStrip | – Có thể dễ dàng kết hợp vào trong các hệ thống xử lý bùn hoạt tính đang sử dụng
– Quá trình linh hoạt: quá trình khử Phospho không bị điều khiển bởi tỷ số BOD/P – Ít sử dụng hóa chất hơn so với sự kết tủa hóa học dòng chính – Có thể đạt đến nồng độ othorpotphat thấp hơn 1,5 mg/l |
– Yêu cầu thêm vôi để kết tủa Phospho
– Yêu cầu oxy hòa tan cao hơn của dịch trộn để ngăn cản sự giải phòng của Phospho trong bể lọc cuối cùng – Đòi hỏi phải có thêm bể cho việc làm sạch – Cặn vôi là một vấn đề cho việc duy trì |
| Phản ứng theo mẻ liên tục (SBR) | – Quá trình rất linh hoạt cho việc kết hợp kết hợp khử Phospho và Nitơ
– Quá trình đơn giản, dễ vận hành – Chất rắn dịch trộn không thể rứa sạch với sự dâng nước |
– Chỉ thích hợp với những dòng chảy nhỏ
– Đòi hỏi phải có các đơn vị thừa – Chất lượng nước đầu ra tùy thuộc vào thiết bị lắng – Thông số thiết kế hạn chế |
II. Xử lý Phospho trong nước thải bằng phương pháp hóa học
Loại bỏ Phospho bằng cách bổ sung hóa chất thì đơn giản và dễ thực hiện. Tuy nhiên, sẽ làm tăng sản lượng bùn, vận hành và bảo trì cần thêm chi phí. Hóa chất được thêm vào nước thải phải được pha trộn tốt, tiếp theo là chất keo tụ và chất rắn loại bỏ bằng cách lắng, lọc, tách màng, hoặc các quá trình tương tự. Các phản ứng hóa học cho phép phân tách Phospho từ pha nước đến pha rắn và sẽ tạo ra lượng Phospho ở mức thấp. Mức Phospho ít hơn 0,1 mgP/L thì luôn đạt được khi thêm vào chất hóa học tại thiết bị lọc được thiết kế tốt. Nồng độ thấp hơn có thể đạt được với việc áp dụng hóa chất tối ưu và loại bỏ các chất rắn hoàn toàn.
Loại bỏ Phospho hóa học sử dụng các phản ứng giữa chất Phospho trong nước và các hợp chất hóa học, các ion kim loại đa hóa trị, để tạo thành kết tủa của phosphate ít hòa tan sau đó có thể được loại bỏ ra khỏi chất lỏng bằng cách sử dụng một quá trình tách chất rắn. Các hóa chất thường được sử dụng là nhôm [Al(III)], sắt [(III) Fe], và canxi [Ca(II)].
BẲNG VÔI
5Ca2+ + 3PO43- + OH– ↔ Ca5(PO4)3(OH)
Mg2+ + 2OH– ↔ Mg(OH)2
Ca2+ + CO32- ↔ CaCO3
BẰNG PHÈN NHÔM
Al3+ + PO43+ ↔ AlPO4
Al3+ + 3OH– ↔ Al(OH)3
BẰNG PHÈN SẮT
Fe3+ + PO43- ↔ FePO4
Fe3+ + 3OH– ↔ Fe(OH)3








